Содержание
Врожденная глаукома диагностируется при прогрессирующем повышении внутриглазного давления, вызванном внутриутробно развившимися дефектами. Внешне распознать патологию можно по увеличенным размерам глазных яблок, светобоязни, повышенной слезоточивости. Характерна болезненность, вызывающая беспокойство у ребенка. При обследовании обнаруживаются астигматизм или близорукость, возможно помутнение роговицы. На фоне высокого давления внутри глаза развиваются необратимые патологические изменения. Без лечения слепота наступит уже через 4-5 лет после появления первых глаукомных признаков.
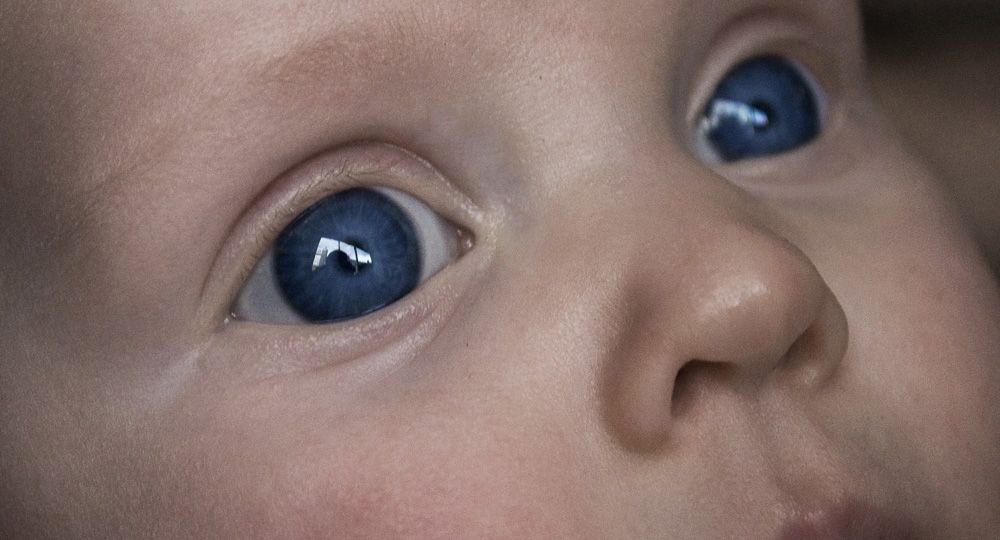
Причины и механизм развития врожденной глаукомы
Более чем в 80% случаев патология возникает из-за генетических мутаций. Поломка CYP1B1 приводит к нарушению структуры кодируемого им белка, который принимает участие в формировании трабекулярной (дренажной) ткани передней камеры глаза. Она расположена в месте соединения радужки и роговицы, которые образуют угол. Мутация передается по наследству аутосомно-рецессивным путем. Такая глаукома называется первичной.
Данная форма не всегда диагностируется при рождении ребенка. Скорость появления симптомов зависит от степени недоразвития трабекулярной ткани. Признаки могут появиться в 3-10 лет (инфантильная форма) или в подростковом возрасте (ювенильная форма).
В 20% случаев развивается вторичная глаукома. Ее причиной являются спонтанные генетические поломки и внутриутробные повреждения зрительного аппарата. Последние нередко возникают вследствие заболеваний матери. Наиболее опасные патологии:
-
краснуха;
-
цитомегаловирус;
-
токсоплазмоз;
-
полиомиелит;
-
грипп.
Причиной внутриутробных повреждений также является тератогенное действие принимаемых матерью препаратов.
Существенным фактором риска является недоношенность. В 70% случаев глаукома у таких детей возникает на обоих глазах.
Механизм развития
Под действием провоцирующих факторов оказывается недоразвитым угол передней камеры глаза, в котором находится трабекулярная сеть. В результате образующаяся внутри глаза влага перестает оттекать по предназначенным для этого каналам.
Жидкость постепенно накапливается и повышает давление внутри глаза. Кровоток в его структурах ухудшается, происходит ишемическое голодание. Сетчатка начинает истончаться, повреждается глазной нерв.
Методы лечения
При выявлении врожденной офтальмогипертензии необходимо регулярное инструментальное обследование для отслеживания динамики. Единственным эффективным методом лечения является хирургическая операция. До нее ребенку капают понижающее давление капли, назначают препараты для улучшения метаболизма и кровообращения.
Существует несколько видов операций. Их задача – восстановление дренажа внутриглазной влаги. Для достижения этой цели есть три пути:
-
Устранение препятствий в существующих путях оттока.
-
Формирование новых путей.
-
Сокращение объема влаги, вырабатываемой цилиарным телом.
Врач выбирает метод хирургического вмешательства на основании данных диагностики. Играет роль прозрачность роговицы, время появления первых симптомов, состояние зрительного нерва.
Гониотомия
Задача – создать прямое сообщение между передней камерой и круговым сосудом (шлеммовым каналом), по которому оттекает жидкость. Для этого удаляют находящуюся между ними дренажную пористую ткань.
Операция выполняется при хорошо просматриваемом угле передней камеры и достаточной прозрачности роговицы. Для улучшения детализации используют гониолинзу. Врач вводит гониотом через переднюю камеру и рассекает трабекулу.
Операция занимает несколько минут и не вызывает осложнений. По истечении 5 лет у 90% пациентов внутриглазное давление остается в норме.
Трабекулотомия (синустрабекулэктомия)
Проведение операции возможно при непрозрачной роговице, а также при аномалиях переднего сегмента глаза. Задача такая же, как у гониотомии, но есть отличия в месте разреза. При трабекулотомии врач выкраивает круговой лоскут в склере и через полученное отверстие формирует канал в дренажной ткани.
Манипуляции производятся при помощи тонкого изогнутого ножа-трабекулотома. Врач вводит его через конъюнктивальный или склеральный разрез в шлеммов канал, создает прямое сообщение между ним и передней камерой. При необходимости для восстановления проходимости канала может быть применено стентирование.
В современной модификации формируется канал между передней камерой и пространством под конъюнктивой. Жидкость оттекает в фильтрационную подушку, а оттуда поступает в кровоток. Во избежание закрытия канала устанавливают шунт.
Лазерная циклофотокоагуляция
Применяется при неэффективности других методов и при наличии противопоказаний к ним.
Задачей процедуры является сокращение количества продуцируемой влаги. Эффект достигается за счет повреждения структуры цилиарного тела и прижигания питающих его сосудов.
В ходе операции в области соединения роговицы и склеры по кругу наносят около 25 точек. Лазерный луч проникает на заданную глубину и не повреждает окружающие ткани.
Циклокриокоагуляция
Процедура аналогична лазерной циклофотокоагуляции, но повреждение цилиарного тела производится при помощи криозонда. На поверхность склеры в проекции цилиарного тела наносится 6-8 точек. Эффект развивается в течение нескольких дней по мере атрофии тканей. При неудовлетворительном результате через 2-3 недели процедуру можно повторить.
Прогноз
Прогноз зависит от того, насколько своевременно начато лечение. Дети с диагностированной глаукомой или подозрением на нее ставятся на учет в поликлинике. Обследования проводятся не реже раза в квартал.
После операции ребенка осматривают через месяц. Затем частота обследований зависит от сложности случая – раз в 1,3 или 6 месяцев.
Подробную информацию о современных методиках лечения врожденной глаукомы можно узнать на сайте https://excimerclinic.ru/babyvision/congenital_glaucoma/.